|
Campionamento e analisi geochimica delle acque
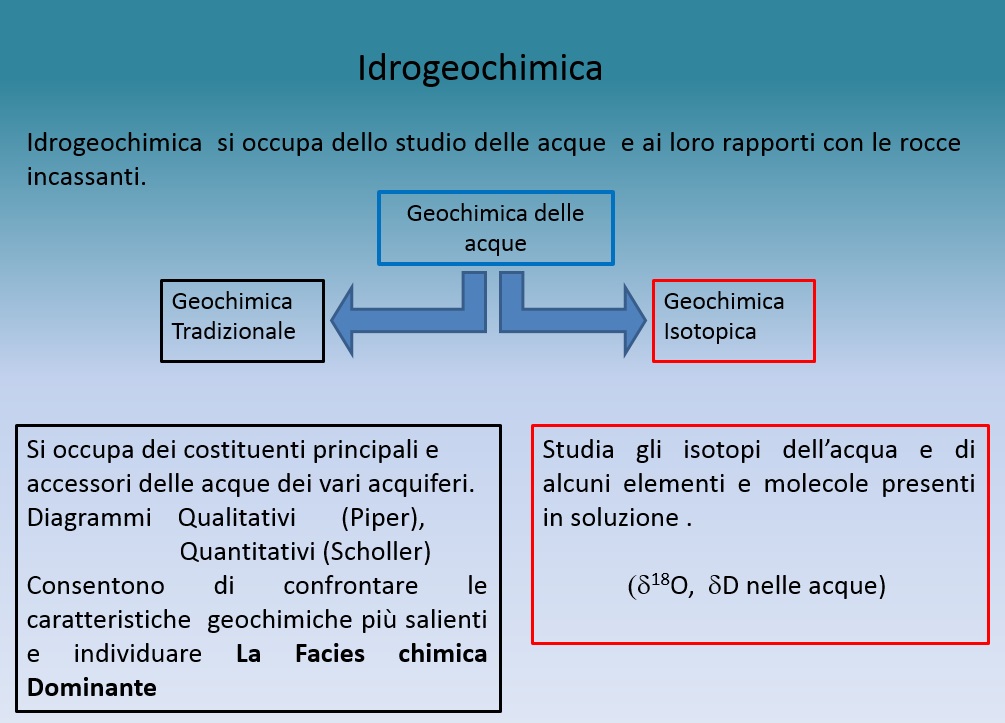
Cenni di Idrogeochimica L’ idrogeochimica si occupa dello studio chimico delle acque sotterranee ed ai loro rapporti con le rocce incassanti. La geochimica delle acque viene divisa in:
|
Studio geochimico di un acqua tramite geochimica tradizionale
La facies chimica è la definizione della famiglia geochimica di appartenenza dell’acqua sotterranea, le acque sono comunemente divise in :
1) Facies Bicarbonato-calcica
2) Facies bicarbonato-calcico-magnesiaca
3) Facies solfato calcica
4) Facies cloruro-alcalina
5) Facies bicarbonato-alcalina
La facies chimica è la definizione della famiglia geochimica di appartenenza dell’acqua sotterranea, le acque sono comunemente divise in :
1) Facies Bicarbonato-calcica
2) Facies bicarbonato-calcico-magnesiaca
3) Facies solfato calcica
4) Facies cloruro-alcalina
5) Facies bicarbonato-alcalina
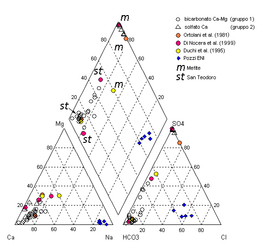
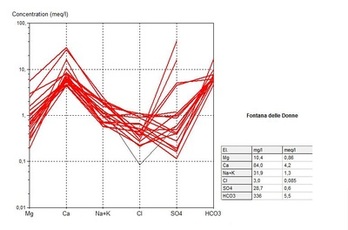
Il chimismo delle acque può essere rappresentato graficamente con diagrammi qualitativi che consentono di confrontare le caratteristiche geochimiche più salienti il più rappresentativo di questi è il diagramma di Piper, e diagrammi quantitativi dove si riportano le concentrazioni analitiche meq/l dei costituenti ionici principali dove il più impiegato è il diagramma di Scholler.
|
L’analisi chimico-fisica di un acqua viene effettuata in parte in situ, tramite strumenti portatili come una sonda multi-parametrica (Fig), e in parte in laboratori attrezzati.
In situ al momento del prelievo del campione si misura la temperatura dell’acqua determinando il grado di termalismo della stessa (vedi tabella 1). |
Fig. Sonda multiparametrica
|
Temperaturura
Oltre alla temperatura è fondamentale misurare anche il PH dell’acqua e la conducibilità elettrica, questo parametro però è in funzione diretta della temperatura e dovrebbe essere di norma riferito alla temperatura standard di 20-25°C.
La conducibilità permette di classificare le acque in:
La conducibilità permette di classificare le acque in:
Tramite la Sonda Multiparametrica inoltre vengono misurati altri parametri quali il potenziale di ossidoriduzione Eh e l’ ossigeno disciolto, i campioni prelevati saranno conservati in frigorifero.
Il potenziale di riduzione misura la tendenza della soluzione elettrolitica a perdere o acquisire elettroni quando la soluzione subisce un cambiamento dovuto all'aggiunta di una nuova specie. Una soluzione con un potenziale di riduzione maggiore (più positivo) rispetto alle specie aggiunte tenderà a guadagnare elettroni a discapito delle nuove specie (cioè sarà ridotta ossidando le nuove specie), mentre una soluzione con un potenziale di riduzione minore tenderà a perdere elettroni, cioè sarà ossidata riducendo le nuove specie.
Poiché i potenziali di riduzione assoluti sono difficili da misurare in maniera precisa, vengono definiti rispetto ad un elettrodo di riferimento. I potenziali di riduzione vengono quindi determinati misurando la differenza di potenziale elettrico fra un elettrodo di lavoro immerso nella soluzione di cui si vuole misurare il valore e un elettrodo di riferimento immerso in un'altra soluzione collegata elettricamente alla prima attraverso un ponte salino. Il valore del potenziale di riduzione associato all'elettrodo di riferimento è noto; ad esempio il potenziale di riduzione dell'elettrodo standard a idrogeno è per convenzione pari 0,0 mV. Per ottenere maggiore stabilità e precisione, durante lo svolgimento dei test di laboratorio si preferisce usare un elettrodo standard a cloruro d'argento oppure un elettrodo a calomelano saturo (SCE).
Le caratteristiche geochimiche di un acqua sotterranea si può limitare ai suoi cationi Ca2+, Mg2+, Na+, K+, e anioni principali HCO3-, SO42-, Cl-, NO3- oltre alla SiO2.
Esprimendo i dati analitici in mg/l, lo ione più abbondate tra i costituenti principali è l’HCO3- seguito da Ca2+, Na+, SO42-, Cl-, ed SiO2, seguono in concentrazioni minori, K+ ed NO3-.
Per un’analisi più completa possono essere determinati anche i costituenti minori presenti in traccia (Litio, Stronzio, Bario, Boro, Ferro, Manganese, Zinco, Mercurio, Rame, Piombo, Nichelio, Cadmio, Cromo, Alluminio, Arsenico, ione Ammonio, ammoniaca, Fosfati, Fluoruri, Bromuri, Ioduri, Solfuri, Nitriti, Cianuri ecc).
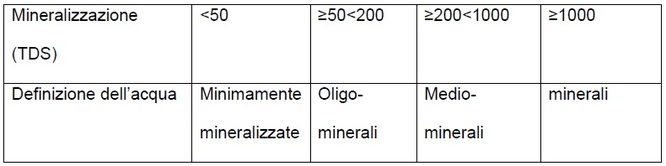
La mineralizzazione di un acqua si esprime con il total dissolved solids (TDS) ed è la somma espressa in mg/l dei cationi (Σ+mg/l), degli anioni (Σ-mg/l), e della silice (SiO2):
TDS(mg/l)=Σ+mg/l + Σ-mg/l+SiO2
Il potenziale di riduzione misura la tendenza della soluzione elettrolitica a perdere o acquisire elettroni quando la soluzione subisce un cambiamento dovuto all'aggiunta di una nuova specie. Una soluzione con un potenziale di riduzione maggiore (più positivo) rispetto alle specie aggiunte tenderà a guadagnare elettroni a discapito delle nuove specie (cioè sarà ridotta ossidando le nuove specie), mentre una soluzione con un potenziale di riduzione minore tenderà a perdere elettroni, cioè sarà ossidata riducendo le nuove specie.
Poiché i potenziali di riduzione assoluti sono difficili da misurare in maniera precisa, vengono definiti rispetto ad un elettrodo di riferimento. I potenziali di riduzione vengono quindi determinati misurando la differenza di potenziale elettrico fra un elettrodo di lavoro immerso nella soluzione di cui si vuole misurare il valore e un elettrodo di riferimento immerso in un'altra soluzione collegata elettricamente alla prima attraverso un ponte salino. Il valore del potenziale di riduzione associato all'elettrodo di riferimento è noto; ad esempio il potenziale di riduzione dell'elettrodo standard a idrogeno è per convenzione pari 0,0 mV. Per ottenere maggiore stabilità e precisione, durante lo svolgimento dei test di laboratorio si preferisce usare un elettrodo standard a cloruro d'argento oppure un elettrodo a calomelano saturo (SCE).
Le caratteristiche geochimiche di un acqua sotterranea si può limitare ai suoi cationi Ca2+, Mg2+, Na+, K+, e anioni principali HCO3-, SO42-, Cl-, NO3- oltre alla SiO2.
Esprimendo i dati analitici in mg/l, lo ione più abbondate tra i costituenti principali è l’HCO3- seguito da Ca2+, Na+, SO42-, Cl-, ed SiO2, seguono in concentrazioni minori, K+ ed NO3-.
Per un’analisi più completa possono essere determinati anche i costituenti minori presenti in traccia (Litio, Stronzio, Bario, Boro, Ferro, Manganese, Zinco, Mercurio, Rame, Piombo, Nichelio, Cadmio, Cromo, Alluminio, Arsenico, ione Ammonio, ammoniaca, Fosfati, Fluoruri, Bromuri, Ioduri, Solfuri, Nitriti, Cianuri ecc).
La mineralizzazione di un acqua si esprime con il total dissolved solids (TDS) ed è la somma espressa in mg/l dei cationi (Σ+mg/l), degli anioni (Σ-mg/l), e della silice (SiO2):
TDS(mg/l)=Σ+mg/l + Σ-mg/l+SiO2